Hinweise zum Experiment
Damit in Chemie bzw. beim Experimentieren keine Unfälle passieren, musst du auf die Sicherheit achten. Die Sicherheit ist immer wichtig, wenn du in einem Fachraum oder Labor bist. Bitte beachte bei allen Experimenten die Hinweise zur Sicherheit im Labor. Die Durchführung des Experiments erfordert eine Gefährdungsbeurteilung durch die Lehrkraft.
Material
- Rundkolben \(\ce{(1000 ml)}\)
- Luftballon
- Gummistopfen, Klebeband etc. um den Luftballon am Rundkolben zu fixieren
- Korkring
- Laborwaage
- Bunsenbrenner
- Klemme
Chemikalien
- Aktivkohle
- Sauerstoff
Edukte
| Stoffname | Summenformel | Gefahrenhinweise |
|---|---|---|
| Sauerstoff | \(\ce {O_2} \) |
H270: Kann Brand verursachen oder verstärken; Oxidationsmittel.
H280: Enthält Gas unter Druck; kann bei Erwärmung explodieren.
P220: Von Kleidung und anderen brennbaren Materialien fernhalten.
P244: Ventile und Ausrüstungsteile öl- und fettfrei halten.
P370+P376: Bei Brand: Undichtigkeit beseitigen, wenn gefahrlos möglich.
P403: An einem gut belüfteten Ort aufbewahren.
|
| Aktivkohle | \(\ce {C}\) |
Kein gefährlicher Stoff nach GHS.
Kein gefährlicher Stoff nach GHS.
|
Produkte
| Stoffname | Summenformel | Gefahrenhinweise |
|---|---|---|
| Kohlenstoffdioxid (als Reaktionsprodukt) | \(\ce {CO_2} \) |
Kein gefährlicher Stoff nach GHS.
P403: An einem gut belüfteten Ort aufbewahren.
|
Versuchsaufbau/Durchführung
Schritt 1
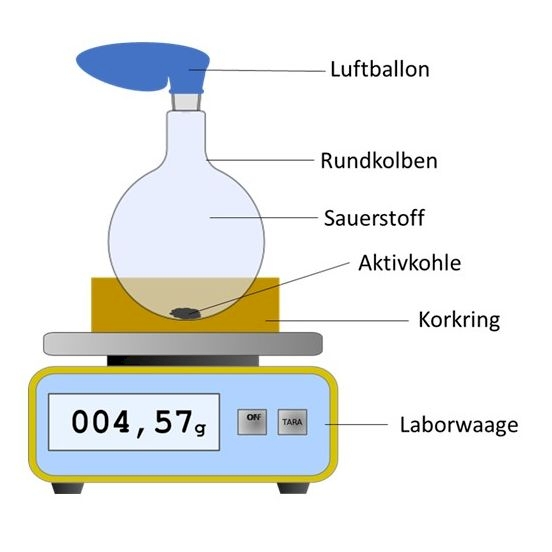
- Stelle den Rundkolben mit dem Korkring auf die Laborwaage.
- Gib etwa \(\ce{200 - 300\,mg}\) Aktivkohle in den Rundkolben.
- Spüle den Rundkolben mit Sauerstoff aus und verschließe den Rundkolben mit dem Luftballon.
- Befestige den Luftballon ggf. mit Klebeband o. ä., um den Luftballon zu fixieren und den Rundkolben luftdicht zu verschließen.
- Wiege nun den Rundkolben mit Luftballon und notiere das Gewicht.
Schritt 2
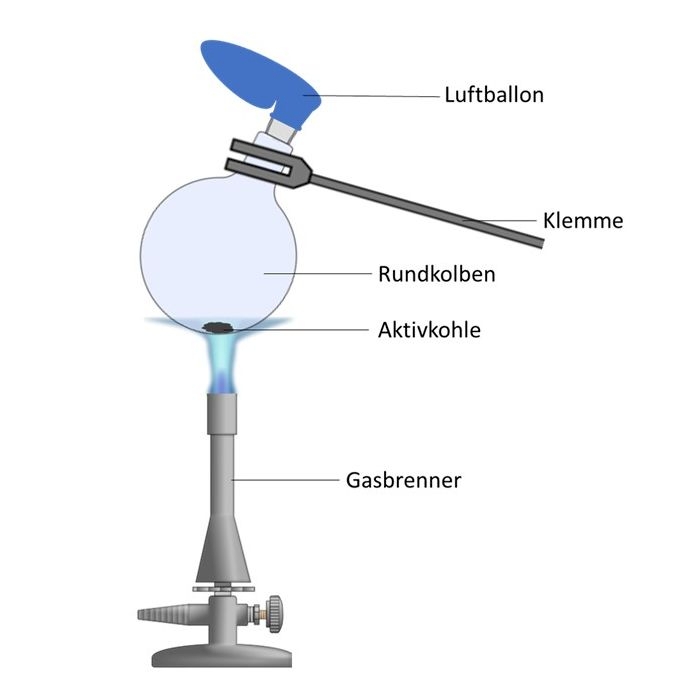
- Befestige die Klammer am Hals des Rundkolbens.
- Zünde die blaue rauschende Flamme des Gasbrenners an.
- Erhitze mit der Brennerflamme die Aktivkohle und schüttle den Rundkolben dabei leicht.
- Höhe auf zu erhitzen, wenn du keine Reste der Aktivkohle mehr sehen kannst.
Schritt 3
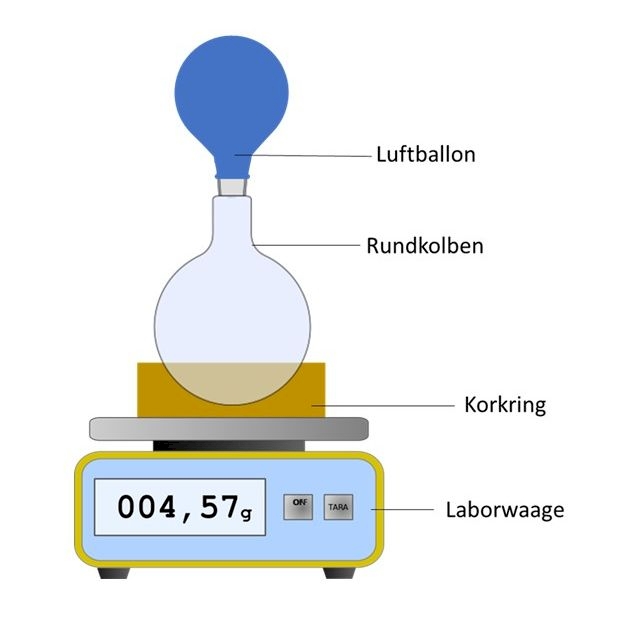
Stelle den Rundkolben mit dem Luftballon wieder auf den Korkring auf der Laborwaage.
Entferne die Klemme und wiege die Masse des Rundkolbens mit dem Luftballon.
Was fällt dir auf?
Aufgabe
Aufgabe
Führe den Versuch durch. Was kannst du beobachten?