Was haben eine Brennnesselpflanze, eine Ameise und ein Wüstenlaufkäfer (Abb. 1) gemeinsam? Sie alle nutzen u.a. Ameisensäure, um sich gegen Feinde zu verteidigen oder auch anzugreifen. Der Wüstenlaufkäfer hat Drüsen am Hinterleib, aus denen er einen Strahl Ameisensäure spitzt, wenn er sich bedroht fühlt. Bei der Brennnessel ist Ameisensäure Bestandteil des Zellsaftes, der in unsere Haut eindringt und brennt, wenn wir eine Brennnessel berühren. Bei den Ameisen wurde bereits im 15. Jahrhundert beobachtet, dass einige Ameisenarten eine saure Flüssigkeit absondern können. Im Jahr 1671 isolierte der Engländer John Ray das erste Mal Ameisensäure. Du fragst dich, wie das genau gemacht wurde? Dann lies in diesem Artikel weiter, der dir mehr über die Ameisensäure, ihre Geschichte, Herstellung und ihre Eigenschaften verrät.
Ameisensäure – die Verteidigungswaffe der Natur
Ameisensäure kommt vielfältig in der Natur vor und wird von Tieren und Pflanzen vor allem als Verteidigungsmittel eingesetzt. Neben den bereits genannten Brennnesseln, Ameisen und Laufkäfern, verwenden auch einige Skorpion-, Raupen-, Quallen- und Bienenarten Ameisensäure zur Verteidigung. Auch in unserem Körper kannst du Ameisensäure finden, denn sie entsteht beispielsweise bei der Verstoffwechselung von Methanol. Zudem ist Ameisensäure auch Bestandteil von Honig und Tabakrauch.
Ameisensäure - auch für uns Menschen nützlich
Ameisensäure wird heutzutage vielfältig verwendet. Anhand der folgenden Auflistung kannst du dir einen Überblick verschaffen.
(Tier-)Medizin:
- Einsatz als Antirheumatikum (entzündungshemmendes und schmerzstillendes Medikament)
- Behandlung von Warzen
- Desinfektion/Abtöten von Bakterien (z.B. zur Verhinderung der Ausbreitung von Tierseuchen)
Industrie:
- Beiz- und Imprägniermittel in der Textil- und Lederindustrie
- Zum Verkleben von Polyamid-Kunststoffen in der Kunststoffindustrie
- Als Reduktionsmittel beim Löten in der Elektronikproduktion
- Entkalkung von Kühlwassersystemen in industriellen Anlagen
Weitere Einsatzgebiete:
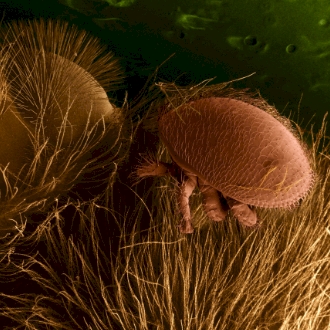
- Imker: Behandlung von Bienen zum Schutz vor Parasiten (Varroamilbe, Abb. 2)
Von der Ameise zur Ameisensäure - Die Geschichte der Ameisensäure-Herstellung
Ameisensäure wurde früher (im 17. Und 18. Jahrhundert) aus Ameisen gewonnen, indem eine große Anzahl an Ameisen destilliert oder mit kochendem Wasser übergossen und ausgedrückt wurden. Zum Glück für die Ameisen wurden im 19. Jahrhundert andere Wege gefunden, um Ameisensäure aus Cyanwasserstoff oder Kohlenmonoxid zu synthetisieren. Die Synthese aus Kohlenmonoxid wurde von Marcellin Berthelot (Abb. 3) erfunden und wird heute noch genutzt. Sie umfasst zwei Schritte.
Im ersten Schritt wird Natriumhydroxid mit Kohlenmonoxid bei einer Temperatur von 130°C und einem Druck von 6-8 bar umgesetzt. Dabei entsteht das Salz Natriumformiat. Die Salze der Ameisensäure nennen wir Formiate; das ist abgeleitet von der lateinischen Bezeichnung "formica" für Ameise.
\(\ce{NaOH + CO -> HCOONa}\)
Im zweiten Schritt wird das Natriumformiat mit Schwefelsäure zur Reaktion gebracht und es entstehen Ameisensäure und das Salz Natriumsulfat.
\(\ce{2 HCOONa + H_2SO_4 -> 2 HCOOH + Na_2SO_4}\)
Bei diesem Reaktionsschritt handelt es sich um eine Verdrängungsreaktion, d.h. die starke Säure (Schwefelsäure) vertreibt die schwache Säure aus ihrem Salz (Natriumformiat). Es bildet sich die schwache Säure (Ameisensäure) und das Salz der starken Säure (Natriumsulfat). Mehr zu Verdrängungsreaktionen findest du hier.
Ameisensäure kann auch noch auf anderen Wegen, z.B. aus Methanol oder als Nebenprodukt bei der Essigsäure-Herstellung, gewonnen werden.
Ameisensäure chemisch betrachtet - Aufbau und Eigenschaften
Ameisensäure ist die einfachste Carbonsäure mit der Summenformel \(\ce{CH_2O_2}\) und der Halbsummenformel \(\ce{HCOOH}\). Sie ist die Alkansäure mit der kürzest möglichen Kette (ein C-Atom), weswegen ihr systematischer Name auch Methansäure lautet (Abb. 4). Ihr \(\ce{pK_s-}\)Wert beträgt 3,77. Sie ist somit eine starke Säure.
Ameisensäure ist eine farblose, klare Flüssigkeit, die einen starken und stechenden Geruch hat. Sie ist relativ instabil und zersetzt sich unter Gasbildung, weswegen konzentrierte Ameisensäure-Lösungen \(\ce{(ω\,>\,85\%)}\) oder reine Ameisensäure in speziellen Flaschen mit Entlüftungsventil aufbewahrt werden müssen. In der Schule sollten nur geringer konzentrierte Ameisensäure-Lösungen aufbewahrt werden.
In der Tabelle (Abb. 5) sind weitere wichtige Eigenschaften der Ameisensäure zusammengefasst:
| Molare Masse | \(\ce{46,03\,\frac{g}{mol}}\) |
| Dichte | \(\ce{1,22\,\frac{g}{cm^3}}\) |
| Schmelzpunkt | \(\ce{8\,°C}\) |
| Siedepunkt | \(\ce{101\,°C}\) |
Auffällig ist bei der Ameisensäure, dass Schmelz- und Siedepunkt höher liegen als bei anderen organischen Stoffen mit einer ähnlichen molaren Masse, wie beispielsweise Propan (Schmelzpunkt: \(\pu{-187,7°\,C}\), Siedepunkt: \(\pu{-42,1°\,C}\), molare Masse: 44,1 \(\ce{\frac{g}{mol}}\)). Dies liegt daran, dass die Ameisensäure Wasserstoffbrücken ausbildet (Abb. 6), welche beim Schmelzen oder Sieden zunächst aufgebrochen werden müssen und dafür wird Energie benötigt.
Die vielseitigen Reaktionen der Ameisensäure
Ameisensäure ist ein starkes Reduktionsmittel, weil sie gleichzeitig einen Aldehyd (Hydroxyformaldehyd) darstellt. Sie verbrennt mit Sauerstoff zu Kohlenstoffdioxid und Wasser.
\(\ce{2HCOOH + O_2 -> 2CO_2 + 2 H_2O}\)
Zudem sollte Ameisensäure im Chemikalienschrank niemals zusammen mit Schwefelsäure aufbewahrt werden, denn in Gegenwart von Schwefelsäure zerfällt Ameisensäure zu Wasser und Kohlenmonoxid.
\(\ce{CHOOH ->[H_2SO_4] CO + H_2O}\)
Mit unedlen Metallen (z.B. Natrium) reagiert Ameisensäure zu einem Salz (Formiat) und Wasserstoff.
\(\ce{2 Na + 2 HCOOH -> 2 HCOONa + H_2}\)
Im alkalischen Milieu reagiert die Ameisensäure mit Silber-Ionen und es bildet sich elementares Silber. Diese Reaktion wird auch als Nachweisreaktion für Ameisensäure eingesetzt, indem beispielsweise eine ammoniakalische Silbernitratlösung mit Ameisensäure zur Reaktion gebracht wird.
\(\ce{HCOOH + 2 Ag^+ + 3 OH^- -> 2 Ag + HCO_3^- + 2 H_2O}\)
Zusammenfassung
Ameisensäure ist die einfachste Alkan-Carbonsäure, die insbesondere im Tierreich als Verteidigungsflüssigkeit eine wichtige Rolle spielt. Sie hat die Summenformel \(\ce{CH_2O_2}\) und ist eine starke Säure. In unserem täglichen Leben spielt sie u.a. in der Industrie und Medizin sowie beim Imkern eine Rolle.
Aufgabe
Aufgabe
Genauso wie andere Carbonsäuren auch, kann auch Ameisensäure mit Alkoholen zu einem Ester reagieren. Die Anwesenheit eines Katalysators, wie Schwefelsäure, ist für die Reaktion notwendig.
Notiere die Reaktionsgleichung für die säurekatalysierte Reaktion von Ameisensäure und Ethanol zu Ameisensäureethylester.